Растущие расходы на отпускаемые по рецепту лекарства являются серьезной проблемой для государственных и частных плательщиков во многих странах. В Соединенных Штатах, продажи рецептурных достиг 300,3 миллиарда $ в 2009 году увеличился на 5,3% по сравнению с предыдущим год.[1] Фармацевтические меры контроля затрат часто включают увеличение пациентов совместного несения расходов, например, с помощью многоуровневого формуляра.[2] Хотя такие подходы эффективно снижают затраты на лекарственные препараты для поставщиков, они также могут быть выгодны для пациентов, чтобы уменьшить их использованию основных лекарственных средств, но это может иметь неблагоприятные клинические последствия, которые могут увеличить, а не уменьшить общие расходы на здравоохранение.[3-6]
В других странах, “референтное ценообразование” используется в качестве инструмента сокращения издержек, который появляется, чтобы не иметь нежелательных последствий для выгоды аптек.[7] Эта стратегия политики устанавливает стандартную цену или компенсации уровня для группы терапевтически взаимозаменяемых препаратов, часто основанные на цене самой низкой стоимости члена в классе. Производители других изделий могут цены на свои продукты выше или ниже этого уровня, и пациенты несут ответственность за любые расходы выше базовой цены. В американском контексте, политика иногда описывается как «максимально допустимая стоимость программы (MAC)».[8]
Справочник цен на лекарства предлагается, как решение политики ценообразования в США.[9] Например, Пирсон и Бах предложили референтное ценообразование, которое используется в страховке, с покрытием и решением, возмещение проинформированных сравнительных исследований эффективности.[10] Хотя американский опыт референтного ценообразования является крайне ограниченным, его широко применяли в мире, началось в Германии в 1989 году, за ней следуют Нидерланды в 1991 году и Новой Зеландии в 1993 году и более чем полдюжины стран, поскольку обеспечивает доказательную базу для оценки его потенциальной роли в США.[11],[12] По данным С.А. Романовой (2014), на фармацевтическом рынке РФ доминируют иностранные производители. Объем производства отечественных лекарственных средств с 2006 г. вырос в 3,3 раза — до уровня 191,699 млрд руб., однако это составляет только 18,3% рынка [42]. Нехватка собственных лекарств покрывается за счет импорта, который с 2006 г. вырос в 2,3 раза и в 2013 г. составил 14,9 млрд долл. (476,7 млрд руб.). Соответственно, мы систематически проанализировали научную литературу, чтобы понять последствия референтного ценообразования на лекарства, используемые плательщиками и расходы пациентов, а также потребление лекарств.
МЕТОДЫ
Мы провели структурированный электронный поиск в рецензируемых журналах с использованием PubMed, Econlit, Embase, Business Source Complete, до мая 2012 года, которые сообщали о влиянии политики ценообразования, ссылки на лекарства, на наличие лекарств ключевых элементов исследования, такие как изучение вопроса, сопоставимость предметов и измерения конечных результатов.
Наша электронная стратегия поиска включала медицинские предметные рубрики и ключевые слова, связанные с фармацевтическими препаратами (например, «экономика, фармацевтическая», «по использованию лекарственных средств» или «сборы, фармацевтические»), политику в области здравоохранения (например, «регулирование государственной политики в сфере здравоохранения», «политика в области здравоохранения» ), и анализ политики (например, «экономика здравоохранения», «стоимость и анализ затрат»), в дополнение к тем, которые конкретно связаны с базовых цен по имени («базовые цены», «справочная цена», «справочник цен на лекарственные средства»). Условия поиска были скорректированы для каждой базы данных, сохраняя при этом общую общую архитектуру.
 Использование предопределенных критериев включения и исключения и тезисы были использованы для выявления потенциально соответствующих статей. Мы извлекали опубликованные версии всех статей и пересмотрели свои списки литературы для выявления дополнительных соответствующих исследований. Обзор был ограничен работами, которые оценивали внедрение политики базовых цен либо на конкретных или всех классов лекарственных средств в рамках системы здравоохранения, в результате чего из исследований, которые оценивали постепенные изменения политики в отношении базовых цен. Кроме того, мы исключили исследования, в которых (1) не оценивать последствия ведения ценовой политики на лекарства, (2) не представили исходные данные, или (3) оценивались нами, как не представляющие интерес.
Использование предопределенных критериев включения и исключения и тезисы были использованы для выявления потенциально соответствующих статей. Мы извлекали опубликованные версии всех статей и пересмотрели свои списки литературы для выявления дополнительных соответствующих исследований. Обзор был ограничен работами, которые оценивали внедрение политики базовых цен либо на конкретных или всех классов лекарственных средств в рамках системы здравоохранения, в результате чего из исследований, которые оценивали постепенные изменения политики в отношении базовых цен. Кроме того, мы исключили исследования, в которых (1) не оценивать последствия ведения ценовой политики на лекарства, (2) не представили исходные данные, или (3) оценивались нами, как не представляющие интерес.
Данные по изучению популяций и характеристик, результатов и качество исследования были извлечены из каждой статьи с использованием стандартного протокола и формы отчетности. Конкретная информация, собранная входит изучение и анализ конструкции (то есть, когорты, поперечное сечение, рандомизированное исследование контроль), разработки политики (т.е. как устанавливается цена на целевые лекарства), образец пациента (т.е. национальных, провинциальных, частных), классы лекарств, дата реализации, и результаты. Результаты исследования были разделены на 3 группы: (1) цены на лекарства, (2) использование, коммутации и соблюдения режима, и (3) расходы и потребление ресурсов. При этом в явном виде не представлены, мы рассчитали процентное изменение в расходах и / или на сбережения населения на основе опубликованных результатов.
Качество исследования было оценено с Агентством по здравоохранению и качеству исследований (AHRQ) 13 инструмента для определения рейтинга наблюдательные исследования когорты. Показатель качества исследования из каждого исследования была рассчитана как доля от общего числа точек, полученных каждой бумаги. Исследования были забиты с максимумом 9 баллов, 1 для каждого домена исследования, где была проведена оценка, и обсуждались результаты.
Наши поиски дали результат в 16 исследованиях, описывающих 9 справочно-ценовых политиках из 6 стран (Рисунок 1).[8],[9],[14-28] Все исследования были опубликованы в последнее десятилетие. Из политики исследованных 1 был применен на региональном уровне в Британской Колумбии, Канада, 2 были применены в частных, финансируемых работодателями планов в области здравоохранения (1 в Канаде и 1 в Соединенных Штатах), а остальные политики были реализованы на национальном уровне в Германии , Норвегия и Испания (таблица 1). 9 политика охватывает 2 типа базовых цен, «родовое базовых цен» и «терапевтическим базовых цен.» Четыре из 9 политики (оцениваемых в 5 из 16 исследований) относились к родовым базовых цен, а другой 5 (11 из 16 исследования) относились к терапевтическому базовых цен. Родовой базовых цен (или «максимально допустимая стоимость») включает в себя только непатентованные лекарства в течение определенного терапевтического класса в то время как терапевтическое базовых цен (или «терапевтическая максимально допустимая стоимость») относится ко всем приемлемых продуктов, onand вне патента, в пределах терапевтического класса.
В Германии, Комитет здравоохранения и фондов медицинского страхования (Committee of healthcare providers and sickness funds), с участием производителей, решает, как лекарства должны быть сгруппированы и устанавливает эталонные цены. Эталонные цены всегда были ниже цены самого высокого продукта стоимости в группе и выше нижней трети цен на рынке.[14] Норвегии и Испании следуют подобной практики и производители могут корректировать свои цены на продукцию в ответ. национальная политика в области ценообразования реферирование Норвегии с тех пор были отменены из-за экономии в расходах были не столь велики, как expected.[15] Регуляторы в Британской Колумбии, Канада, выбрать конкретные продукты, чтобы быть препараты сравнения, а не установить базовую цену. Независимый консультативный комитет решает, какой терапевтической группы продуктов будет зависеть от программы, а также продукты, которые не будут сталкиваться любой распределение расходов в соответствии с эталонным прайсом.[18] В Канаде программа справочная цена на нестероидные противовоспалительные препараты (НПВП) была представила в течении 18 месяцев после того, как общая политика замещения была введена в действие для того же класса.[17] В Испании, некоторых других затрат и сдерживания политики, были реализованы во время введения системы референтного ценообразования в 2000 году, в том числе торговая наценка корректировки цен, полученных производителем, оптовиками и аптеками в 1999 и 2000 годах и обязательное снижение отпускных цен в 1999 году и 2000 году.[28] Никакой другой политики для параллельных изменений.
Исследования, как правило, хорошего методологического качества, с баллами в пределах от 56% до 100% по шкале AHRQ (в среднем 82%).
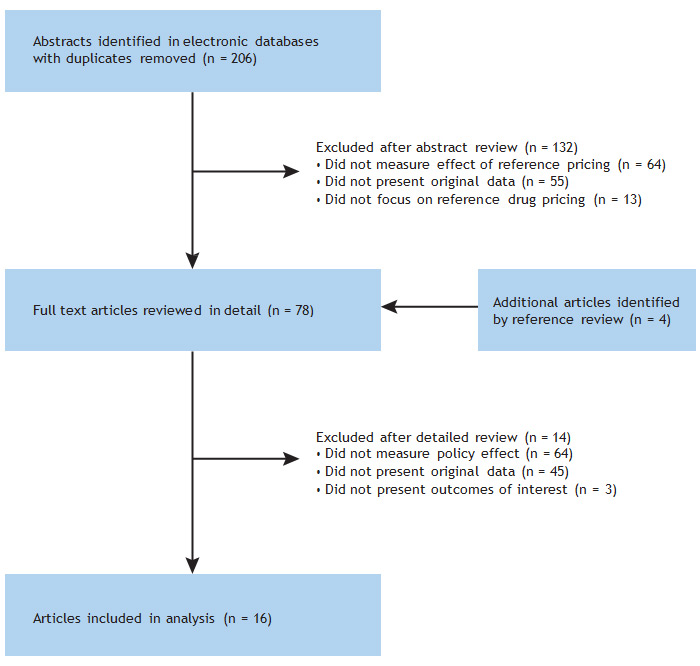
Рисунок 1. Схема исследования выбора
ОБСУЖДЕНИЕ
Наш мета-анализ 16 исследований по оценке влияния политики 9 базовых цен предполагает, что эта стратегия сокращения цен на медикаменты, увеличение использования и соблюдения целевых лекарственных средств, а также способствовало переключение поведения от дорогих продуктов на альтернативы на уровне или ниже базовой цены. Эти результаты были связаны со значительным сокращением как пациента, из собственного кармана и общих расходов плательщика. Хотя частота посещений врача увеличилась в течение короткого периода после реализации политики, не были последовательно наблюдается сокращение посещений и госпитализаций в течение более длительного периода времени. Таким образом, политика, казалось, достичь экономии без негативного влияния на потребление ресурсов. Кроме того, исследование Морено-Торреса на дополнительных эффектах базовых цен в Испании свидетельствует о том, что в то время как общая ссылка ценообразование сокращение расходов плательщика путем включения фирменного наименования продуктов одного и того же активного ингредиента в политике базовых цен на душу фармацевтических расходов также снизились, пользу страховщиков и потребители (4,06 € экономии средств на душу населения, то есть экономия 1,54%).[28]
Справочник цен, как представляется, имеют эффект отличается от многих других стратегий по сдерживанию расходов по рецепту лекарств. В то время, как рецептурные пределы границ защищают плательщиков от чрезмерной стоимости, пределы не могут различать с медицинской точки зрения необходимости и ненужности употребления лекарств и может отговорить пациентов от приобретения лекарств, которые им необходимы. Среди больных, с низким уровнем дохода, у пациентов пожилого возраста, есть проблемы, которые приводят к повышенному риску госпитализации.[30] Терапевтический обмен является широко используемым процедурой, которая позволяет фармацевтам заменить бренд название продукта для типичного продукта из того же терапевтического класса лекарственных средств. Экономия в расходах плательщиков наблюдая в условиях, в которых были реализованы терапевтические обмены, особенно в рамках помощи ветеранам.[31-34] Однако успех терапевтического обмена зависит от активного сотрудничества врачей, потребителей и аптек. Таким образом, некоторые американские планы обнаружили, что терапевтический обмен не был столь же эффективным, как хотелось бы, особенно в оказании влияния на врачей.[35] Практически все публично и в частном порядке застрахованные лица в Соединенных Штатах получают возмещение на основе планов, которые включают многоуровневые формуляры, [36], которые создают стимулы для пациентам использовать общие лекарства или более дешевые фирменные препараты, для которых были договорные скидки.[37] Их введение было показано, что приводит к снижению расходов на лекарства поставщикам, но увеличивают расходы для пациентов и привести к разрывам при использовании в некоторых случаях.[38,39]
Реализация базовых цен в Соединенных Штатах потенциально может происходить несколькими различными способами. Например, в соответствии с действующим в интересах сравнительной эффективности, Пирсон и Бах требуют Medicare для использования базовых цен для установки покрытия и возмещения standards.[10] В рамках этой парадигмы, справка цена будет установлена для новых продуктов сопоставимой клинической эффективности. Хотя законодательство Закон Доступное уход запрещает использование сравнительной эффективности в принятии решений покрытия, закон не по всей видимости, позволит результаты исследований, которые будут использоваться для установления ставок возмещения в рамках более крупной, «итеративной и прозрачного процесса, который включает в себя комментарии общественности и считает, эффект на субпопуляции.»[10] По мере того как немецкий и испанский опыт показывает, это может быть сделано путем поэтапного подхода, в первую очередь реализации базовых цен лишь на несколько классов лекарственных средств, таких как статины и ингибиторы протонной помпы, перед масштабированием до включать более классов.[14,28]
 В качестве альтернативы базовых цен может быть встроен в многоуровневую систему формуляров. Например, в отличие от размещения всех генериков в самом нижнем ярусе стимулирования формуляров, как в настоящее время практикуется, 1 генерик в каждом терапевтического класса можно было бы установить в качестве препарата референтного и цены других генериков, установленных в соответствии с этим. Для фирменных продуктов, базовых цен можно было бы использовать, чтобы установить такую же цену на несколько продуктов в той же терапевтического класса. В настоящее время предпочтительные цены устанавливаются путем переговоров между руководством и выплатами аптечным производителям и только одно фирменное наименование продукта в каждый классе, имеющее привилегированный статус. Установив фиксированный уровень возмещения, более чем 1 продукт может эффективно получить предпочтительный статус, что делает цены более конкурентоспособными и увеличением прозрачность переговоров цены и процесс настройки. С другой стороны, этот процесс может устранить стимулы для производителей, чтобы предоставить руководителям аптек льгот со скидкой в обмен на привилегированную формулярной статуса, и, таким образом, применение базовых цен на фирменной продукции может иметь нечеткие последствия для ценообразования.
В качестве альтернативы базовых цен может быть встроен в многоуровневую систему формуляров. Например, в отличие от размещения всех генериков в самом нижнем ярусе стимулирования формуляров, как в настоящее время практикуется, 1 генерик в каждом терапевтического класса можно было бы установить в качестве препарата референтного и цены других генериков, установленных в соответствии с этим. Для фирменных продуктов, базовых цен можно было бы использовать, чтобы установить такую же цену на несколько продуктов в той же терапевтического класса. В настоящее время предпочтительные цены устанавливаются путем переговоров между руководством и выплатами аптечным производителям и только одно фирменное наименование продукта в каждый классе, имеющее привилегированный статус. Установив фиксированный уровень возмещения, более чем 1 продукт может эффективно получить предпочтительный статус, что делает цены более конкурентоспособными и увеличением прозрачность переговоров цены и процесс настройки. С другой стороны, этот процесс может устранить стимулы для производителей, чтобы предоставить руководителям аптек льгот со скидкой в обмен на привилегированную формулярной статуса, и, таким образом, применение базовых цен на фирменной продукции может иметь нечеткие последствия для ценообразования.
Конечно, эти механизмы введения базовых цен в системе здравоохранения США усложняют пациентов планам с установленными выплатами, которые также могут подорвать преимущества, что стратегия политики предлагает. Отрадно, что введение базовых цен наркотиков в других условиях не оказывает неблагоприятного воздействия на здоровье пациента результаты и использование.
В конечном счете, реализация базовых цен может быть в соответствии с текущими усилиями в Соединенных Штатах, чтобы увеличить значение[40] здравоохранения, например, в то время как стоимость на основе конструкции страхования, как правило, опускают разделение затрат на услуги с высокой добавленной стоимостью, есть много интереса со стороны сообщества поставщиков в разработке методов более экономичного разделения для малоценного сервиса.[41] Установив базовую цену для всех терапевтически эквивалентных мер, эта стратегия создает стимулы для пациентов, чтобы уменьшить их использование этих конкретных услуг, которые являются наиболее дорогостоящими, и, следовательно, имеют наименьшее значение.
Объем базовых цен может быть гораздо шире, чем отпускаемых по рецепту лекарств, и может, на самом деле, более легко применимы и к другим медицинским услугам. Например, плательщики могут установить базовую цену, или фиксированный уровень возмещения, на колоноскопию, основываясь на предположении, что, когда выполняется различными поставщиками по тем же показаниям эта процедура должна иметь равную диагностическую эффективность.
Наше исследование ограничивается коротким сроки многих исследований и относительно ограниченные данные о клинических эффектах политики. Кроме того, исследования различаются по многим важным параметрам, включая размер выборки, базовой методологии и результатов измерений. Каждая страна выполнила свою ценовую политику ссылка на базовой линии другой системы здравоохранения, и обобщаемость какой-либо конкретной стране является сложной задачей. В результате, нам не удалось объединить данные по исследованиям в целях получения сводных мер воздействия базовых цен. Кроме того, принимая во внимание отсутствие сравнительных данных об эффективности на различных направлений политики сдерживания расходов, было трудно сравнить политику и решить добавочную стоимость добавления одной политики сдерживания роста расходов на другую. Другим ограничением является то, что результаты этой политики ссылка наркотиков могут быть специфическими для, и, в зависимости от класса препаратов. Таким образом, хорошие результаты в одном классе эталонным цен на лекарственные средства не могут перевести на хорошие результаты в другой. Тем не менее, наш обзор выявил существенную рецензируемых литературу по данной стратегии политики, которая обеспечивает эмпирическую базу для принятия политических решений. Исходя из этого, ценообразование ссылка наркотиков, как представляется, является эффективным инструментом для контроля расходов на лекарственные средства для частных и государственных плательщиков. В отличие от других механизмов контроля затрат, базовых цен сокращает расходы без отрицательного влияния на использование лекарства или потребление ресурсов. Таким образом, базовые цены могут быть полезными для политики более широкого применения в Соединенных Штатах.
Используемые источники
1. Gatyas G. IMS Health reports U.S. prescription sales grew 5.1 per- cent in 2009, to $300.3 billion [press release]. IMS Health; 2010.
2. Kaiser Family Foundation and Health Research & Educational Trust. Employer Health Benefits 2010 Annual Survey. Menlo Park, CA; 2010.
3. Goldman DP, Joyce GF, Zheng Y. Prescription drug cost sharing: as- sociations with medication and medical utilization and spending and health. JAMA. 2007;298(1):61-69.
4. Schneeweiss S, Patrick AR, Maclure M, Dormuth CR, Glynn RJ. Adherence to statin therapy under drug cost sharing in patients with and without acute myocardial infarction: a population-based natural experiment. Circulation. 2007;115(16):2128-2135.
5. Sokol MC, McGuigan KA, Verbrugge RR, Epstein RS. Impact of medication adherence on hospitalization risk and healthcare cost. Med Care. 2005;43(6):521-530.
6. Osterberg L, Blaschke T. Adherence to medication. N Engl J Med. 2005;353(5):487-497.
7. Schneeweiss S. Reference drug programs: effectiveness and policy implications. Health Policy. 2007;81(1):17-28.
8. Mabasa VH, Ma J. Effect of a therapeutic maximum allowable cost (MAC) program on the cost and utilization of proton pump inhibitors in an employer-sponsored drug plan in Canada. J Manag Care Pharm. 2006;12(5):371-376.
9. Grootendorst PV, Marshall JK, Holbrook AM, Dolovich LR, O’Brien BJ, Levy AR. The impact of reference pricing of nonsteroidal anti- inflammatory agents on the use and costs of analgesic drugs. Health Serv Res. 2005;40(5, pt 1):1297-1317.
10. Pearson SD, Bach PB. How Medicare could use comparative effec- tiveness research in deciding on new coverage and reimbursement. Health Aff (Millwood). 2010;29(10):1796-1804.
11. Danzon PM, Ketcham JD. Reference pricing of pharmaceuticals for Medicare: evidence from Germany, The Netherlands, and New Zealand. Front Health Policy Res. 2004;7:1-54.
12. Galizzi MM, Ghislandi S, Miraldo M. Effects of reference pricing in pharmaceutical markets: a review. Pharmacoeconomics. 2011;29(1): 17-33.
13. West S, King V, Carey TS, et al. Systems to rate the strength of sci- entific evidence. Evid Rep Technol Assess (Summ). 2002;(47):1-11.
14. Augurzky B, Gohlmann S, Gress S, Wasem J. Effects of the German reference drug program on ex-factory prices of prescription drugs: a panel data approach. Health Economics. 2009;18(4):421-436.
15. Brekke KR, Grasdal AL, Holmas TH. Regulation and pricing of pharmaceuticals: reference pricing or price cap regulation? European Economic Review. 2009;53(2):170-185.
16. Grootendorst PV, Dolovich LR, Holbrook AM, Levy AR, O’Brien BJ. The Impact of Reference Pricing of Cardiovascular Drugs on Health Care Costs and Health Outcomes: Evidence from British Columbia— Volume II: Technical Report: McMaster University Quantitative Studies in Economics and Population Research Reports 2002 Quantitative.
17. Grootendorst PV, Marshall JK, Holbrook AM, Dolovich LR, O’Brien BJ, Levy AR. The Impact of Differential Cost Sharing of Non-Steroidal Anti-Inflammatory Agents on the Use and Costs of Analgesic Drugs: McMaster University Social and Economic Dimensions of an Aging Population Research Papers 2004 Social.
18. Hazlet TK, Blough DK. Health services utilization with reference drug pricing of histamine(2) receptor antagonists in British Columbia elderly. Med Care. 2002;40(8):640-649.
19. Pavcnik N. Do pharmaceutical prices respond to insurance? Nat- ional Bureau of Economic Research Working Paper Series. 2000; No. 7865 (published as Pavcnik, N. Do pharmaceutical prices respond to potential patient out-of-pocket expenses? Rand Journal of Economics. 2002, v33 [3, Autumn], 469-487).
20. Puig J. The impact of generic reference pricing interventions in the statin market: Department of Economics and Business Universitat Pompeu Fabra Economics Working Papers 2005.
21. Puig-Junoy J. Incentives and pharmaceutical reimbursement reforms in Spain. Health Policy. 2004;67(2):149-165.
22. Schneeweiss S, Dormuth C, Grootendorst P, Soumerai SB, Maclure M. Net health plan savings from reference pricing for angiotensin- converting enzyme inhibitors in elderly British Columbia residents. Med Care. 2004;42(7):653-660.
23. Schneeweiss S, Maclure M, Soumerai SB. Prescription duration after drug copay changes in older people: methodological aspects. J Am Geriatr Soc. 2002;50(3):521-525.
24. Schneeweiss S, Soumerai SB, Maclure M, Dormuth C, Walker AM, Glynn RJ. Clinical and economic consequences of reference pricing for dihydropyridine calcium channel blockers. Clin Pharmacol Ther. 2003;74(4):388-400.
25. Schneeweiss S, Walker AM, Glynn RJ, Maclure M, Dormuth C, Soumerai SB. Outcomes of reference pricing for angiotensin-convert- ing-enzyme inhibitors. N Engl J Med. 2002;346(11):822-829.
26. Stargardt T. The impact of reference pricing on switching behaviour and healthcare utilisation: the case of statins in Germany. European Journal of Health Economics. 2010;11(3):267-277.
27. Johnson JT, Neill KK, Davis DA. Five-year examination of utiliza- tion and drug cost outcomes associated with benefit design changes including reference pricing for proton pump inhibitors in a state em- ployee health plan. J Manag Care Pharm. 2011;17(3):200-212.
28. Moreno-Torres I, Puig-Junoy J, Raya JM. The impact of repeated cost containment policies on pharmaceutical expenditure: experience in Spain. Eur J Health Econ. 2011;12(6):563-573.
29. Puig-Junoy J. The impact of generic reference pricing interventions in the statin market. Health Policy. 2007;84(1):14-29.
30. Soumerai SB, Ross-Degnan D, Avorn J, McLaughlin T, Choodnovs- kiy I. Effects of Medicaid drug-payment limits on admission to hospi- tals and nursing homes. N Engl J Med. 1991;325(15):1072-1077.
31. Meissner B, Dickson M, Shinogle J, Reeder CE, Belazi D, Senevi- rante V. Drug and medical cost effects of a drug formulary change with therapeutic interchange for statin drugs in a multistate managed Medicaid organization. J Manag Care Pharm. 2006;12(4):331-340.
32. Moisan J, Vaillancourt R, Gregoire JP, Gaudet M, Cote I, Leach A. Preferred hydroxymethylglutaryl-coenzyme A reductase inhibitors: treatment-modification program and outcomes. Am J Health Syst Pharm. 1999;56(14):1437-1441.
33. Patel RJ, Gray DR, Pierce R, Jafari M. Impact of therapeutic inter- change from pravastatin to lovastatin in a Veterans Affairs Medical Center. Am J Manag Care. 1999;5(4):465-474.
34. Korman L, Borysiuk L. Replacing lovastatin with pravastatin: effect on serum lipids and costs. Am J Health Syst Pharm. 1995;52(10): 1078-1082.
35. Wallack SS, Weinberg DB, Thomas CP. Health plans’ strategies to control prescription drug spending. Health Aff (Millwood). 2004;23(6): 141-148.
36. Kaiser Family Foundation and Health Research & Education Trust. Employer Health Benefits Annual Survey. 2010.
37. Rector TS, Finch MD, Danzon PM, Pauly MV, Manda BS. Effect of tiered prescription copayments on the use of preferred brand medica- tions. Med Care. 2003;41(3):398-406.
38. Huskamp HA, Deverka PA, Landrum MB, Epstein RS, McGuigan KA. The effect of three-tier formulary adoption on medication continua- tion and spending among elderly retirees. Health Serv Res. 2007;42(5): 1926-1942.
39. Motheral B, Fairman KA. Effect of a three-tier prescription copay on pharmaceutical and other medical utilization. Med Care. 2001;39(12): 1293-1304.
40. Robinson JC. Applying value-based insurance design to high-cost health services. Health Aff (Millwood). 2010;29(11):2009-2016.
41. Choudhry NK, Rosenthal MB, Milstein A. Assessing the evidence for value-based insurance design. Health Aff (Millwood). 2010;29(11): 1988-1994.
42. Романова С.А. Фармацевтическая промышленность за 2013 г. // Ремедиум 2014. № 3. С. 54-59.
